EGFR突變肺癌:抗體偶聯藥物,疾病控制率可達70%
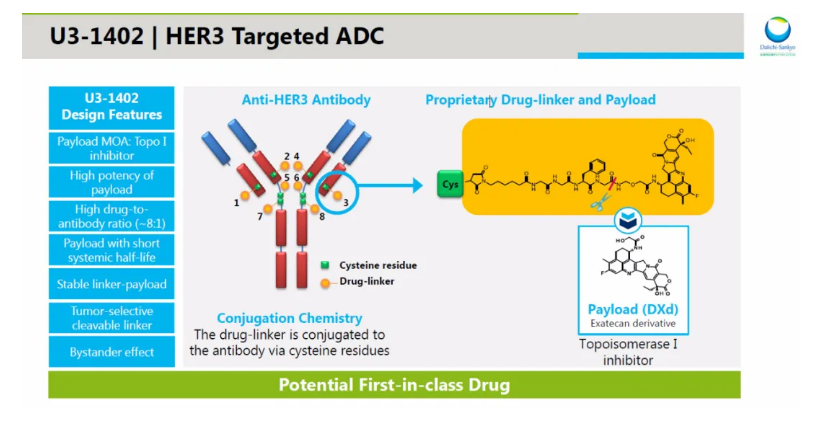
發布日期:2021-02-03HER3在超過80%的EGFR突變型NSCLC中表達,且過表達與不良預后相關。Patritumab deruxtecan (U3-1402)是一種新型的HER3定向ADC,它由單克隆抗體patritumab,一個基于四肽的接頭和一個拓撲異構酶I抑制劑有效載荷組成。
近日舉行的國際肺癌大會,一項1期試驗(NCT03260491)的結果顯示,Patritumab Deruxtecan(U3-1402)在既往接受治療的轉移性或不可切除的EGFR突變非小細胞肺癌(NSCLC)的患者中證明了早期臨床意義。
1期研究包括劑量遞增和劑量擴展階段。在劑量遞增階段,患有轉移性或不可切除的EGFR突變型NSCLC的患者既往接受奧西替尼治療進展、或厄洛替尼,吉非替尼或阿法替尼治療后T790M陰性,每3周接受一次patritumab deruxtecan 5.6mg/kg。在劑量擴展隊列中,轉移性或不可切除的EGFR突變型NSCLC患者,患者既往接受至少1個先前的EGFR TKI和至少1個先前的鉑類化療,每3周接受一次patritumab deruxtecan 5.6mg/kg。評價抗腫瘤活性是本研究的主要終點。將該試劑的安全性和耐受性評估為次要終點。
晚期或轉移性疾病患者接受先前治療的中位數為4(范圍1-9)。先前的治療方法包括奧西替尼(n=49;86%),另一種EGFR靶向治療(n=3;5%),鉑類化療(n=51;90%)和抗PD-1/PD-L1治療(n=23;40%)。大約一半的患者(n=27;47%)有中樞神經系統轉移病史。
截至2020年4月30日,已經對57例來自劑量增加和劑量增加部分的EGFR突變型NSCLC患者進行了Patritumab Deruxtecan治療,其中56例可評估療效。HER3定向的抗體-藥物偶聯物(ADC)在5.6mg/kg劑量下也具有可控的安全性。結果顯示:客觀緩解率為25%,其中包括2%的完全緩解率(n=1)和23%的部分緩解率(n=13)。穩定的疾病率為45%(n=25)。疾病控制率為70%(n=39;95%CI,55.9%-81.2%)。中位反應時間為2.0個月(范圍1.2-2.8),中位持續反應時間為6.9個月(范圍3.0-7.0)。
還進行了一項探索性生物標志物分析,報告稱幾乎所有可評估的患者腫瘤(n=43)在基線時均表達膜HER3。此外,在患者的治療前腫瘤組織和循環腫瘤DNA(ctDNA)中發現了異源EGFR TKI耐藥機制。據報道,具有多種TKI抵抗機制的患者有臨床反應,包括EGFRT790M突變(53%),MET擴增(8%),ERBB2(HER2)突變(4%),BRAF融合,EGFR C797S突變和PIK3CA突變2。其他突變包括HER3突變(2%),HER4突變(8%),CDKN2A突變(6%)和NTRK2突變(2%)。所有接受檢查的患者樣品在康治療后均顯示ctDNA中EGFR激活突變的減少。經歷證實的臨床反應的患者更有可能在第3周或第6周的ctDNA清除EGFR激活突變。未能清除ctDNA的EGFR激活突變與進展性疾病的總體反應有關。
“在既往經過大量治療的患者中觀察到早期抗腫瘤活性,平均隨訪時間為5個月,”紀念斯隆凱特琳癌癥中心Helena A.Yu醫生說,“這些數據支持在沒有可用靶向治療的患者人群中對該HER3定向ADC進行進一步的臨床研究。”HERTHENA-Lung01 2期研究計劃于2021年初啟動,將評估EGFR TKI和鉑類化學療法失敗后患者單藥patritumab deruxtecan的療效。





