KRAS突變肺癌:Rigosertib聯(lián)合免疫顯示有效
發(fā)布日期:2021-07-08根據(jù)正在進(jìn)行的 1/2a 期試驗(yàn) (NCT04263090) 的更新,由rigosertib+nivolumab顯示出對(duì)晚期轉(zhuǎn)移性KRAS突變的非小細(xì)胞肺癌 (NSCLC)患者具有潛在抗癌活性的初步證據(jù)。
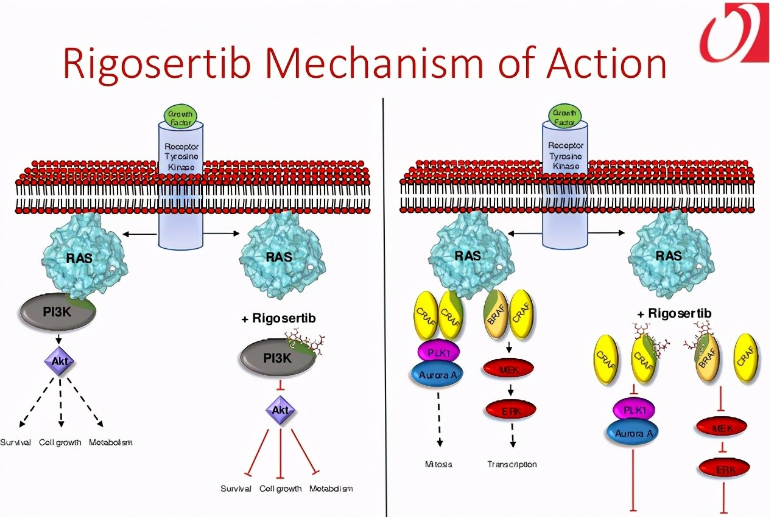
Rigosertib 是一種多激酶抑制劑和選擇性抗癌劑,非 ATP 競(jìng)爭(zhēng)性 PLK1 抑制劑,通過抑制 PI3K/Akt 途徑誘導(dǎo)細(xì)胞凋亡,促進(jìn)組蛋白 H2AX 的磷酸化并誘導(dǎo)細(xì)胞周期中的 G2/M 期停滯。
開放標(biāo)簽 1/2a 期研究招募了 18 歲或以上的患者,這些患者在組織學(xué)或細(xì)胞學(xué)上確診為 IV 期轉(zhuǎn)移性肺腺癌,并且在使用 PD-1 單藥或與鉑雙藥化療后出現(xiàn)進(jìn)展。患者還需要根據(jù) RECIST v1.1 標(biāo)準(zhǔn)和研究者評(píng)估具有可測(cè)量的疾病、至少 3 個(gè)月的預(yù)期壽命。他們不能接受任何其他研究藥物或患有攜帶EGFR突變或ALK易位的腫瘤。患者也不能有未經(jīng)治療的中樞神經(jīng)系統(tǒng)轉(zhuǎn)移或癌性腦膜炎。
該試驗(yàn)由 2 個(gè)階段組成:劑量遞增階段 1 部分和劑量擴(kuò)展階段 2a 部分。研究參與者在d1-21每天兩次口服 rigosertib,并在 28 天治療周期的d1和的d15以 240 mg的固定劑量靜脈注射納武單抗。Rigosertib 目前正在接受以下 3 個(gè)劑量水平的檢查:每天兩次 280 毫克,早上 560 毫克和晚上 280 毫克,以及每天兩次 560 毫克。該試驗(yàn)的主要終點(diǎn)是確定 MTD 和該方案實(shí)現(xiàn)的總體反應(yīng)率。關(guān)鍵的次要終點(diǎn)包括無進(jìn)展生存期和總生存期。
在試驗(yàn)的劑量遞增階段正在評(píng)估的 3 個(gè)隊(duì)列中,尚未達(dá)到雙藥的耐受劑量 (MTD)。值得注意的是,參加該試驗(yàn)的參與者之前曾接受過多種治療方法,并且在各種免疫檢查點(diǎn)抑制劑組合方面出現(xiàn)了進(jìn)展。
研究人員繼續(xù)招募患者進(jìn)入試驗(yàn)的擴(kuò)展階段,以檢查當(dāng)前方案中定義的口服 rigosertib更高劑量。根據(jù)積極的初步數(shù)據(jù),正在準(zhǔn)備一項(xiàng)協(xié)議修正案,以允許評(píng)估增加的 rigosertib 劑量與全劑量納武單抗的組合。
1/2a 期試驗(yàn)的初步結(jié)果非常令人鼓舞,并證明 rigosertib 有潛力通過克服KRAS突變的肺腺癌中的檢查點(diǎn)抑制劑耐藥性來解決關(guān)鍵的未滿足醫(yī)療需求。
我們對(duì)迄今為止從KRAS 突變的非小細(xì)胞肺癌試驗(yàn)中看到的安全性和初步療效信號(hào)感到非常滿意,考慮到這些患者中的許多以前都失敗了多線治療,包括各種組合的檢查點(diǎn)抑制劑。我們支持?jǐn)U大 rigosertib 劑量遞增的計(jì)劃,以確定該組合的推薦 2 期劑量。





