研究表明新的治療策略可減少患者心血管疾病
發布日期:2022-12-29紐約紀念斯隆凱特琳癌癥中心(MSKCC)的研究人員發現,常見的癌癥治療,如放療或蒽環類藥物,通過激活關鍵的炎癥信號通路,對心臟組織造成長期損害。這項發表在《實驗醫學雜志》(JEM)上的研究表明,抑制這一途徑可以減少癌癥幸存者晚年患心臟病的幾率。
許多癌癥都是用輻射和/或藥物治療的,這些藥物通過破壞腫瘤細胞的DNA來殺死腫瘤細胞。但這些治療也會損害患者健康細胞的DNA。隨著癌癥患者的生存率不斷上升,這一長期后果越來越引起人們的關注。例如,放射治療或一類被稱為蒽環類的DNA損傷藥物可能會對心臟產生延遲毒性作用,增加患心血管疾病的風險,包括冠狀動脈疾病或心力衰竭。
一項研究發現,長期存活的霍奇金淋巴瘤患者心血管疾病的發生率是普通人群的5倍。MSKCC的放射腫瘤學家亞當·M·施密特(Adam M.Schmitt)表示:“DNA損傷導致癌癥治療數年后晚期組織毒性的機制尚不清楚。”“識別毒性的致病機制及其激活的早期生物標志物,將為干預治療以預防毒性提供機會。”
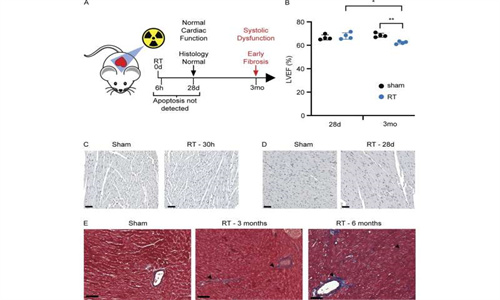
在他們的研究中,施密特和同事們發現,在小鼠暴露于輻射或蒽環類藥物一個月后,一種稱為成纖維細胞的特定心臟細胞群激活了一組基因,這些基因促進了與病理性炎癥和組織纖維化相關的各種免疫細胞類型的募集。在3-6個月內,這些小鼠出現了心臟功能不全的癥狀,到12個月時,許多小鼠死于心力衰竭。
研究人員確定,這種病理過程是由一種稱為cGAS–STING通路的免疫信號通路驅動的。這一途徑通常通過對來自致病細菌或病毒的DNA片段的反應促進炎癥,但Schmitt及其同事推斷,它也可能被輻射或蒽環類藥物治療產生的DNA片段激活。
缺乏cGAS或STING蛋白的小鼠被保護免受DNA損傷癌癥治療的毒性副作用。他們沒有表現出心臟炎癥的跡象,保持了正常的心臟功能,治療一年后仍然活著。STING蛋白的小分子抑制劑也保護小鼠免受放射治療或蒽環類藥物的毒性影響。
通過研究蒽環類藥物治療的乳腺癌患者,Schmitt和同事發現了cGAS–STING途徑在人類心臟毒性中可能發揮同樣重要作用的證據。cGAS–STING信號誘導的關鍵炎癥蛋白之一是CXCL10,研究人員發現,蒽環類藥物治療后CXCL10水平增加更多的患者隨后在超聲心動圖上顯示出與心臟毒性相關的變化。
Schmitt說:“總之,我們的數據表明,cGAS–STING通路的靶向性在預防DNA損傷癌癥治療的心臟并發癥方面具有巨大潛力。這些數據表明,使用cGAS–STING抑制劑預防DNA損傷癌癥治療后心血管疾病的臨床試驗是有必要的。”





