轉移性胰腺癌:中國患者赴美參加了哪些臨床試驗?
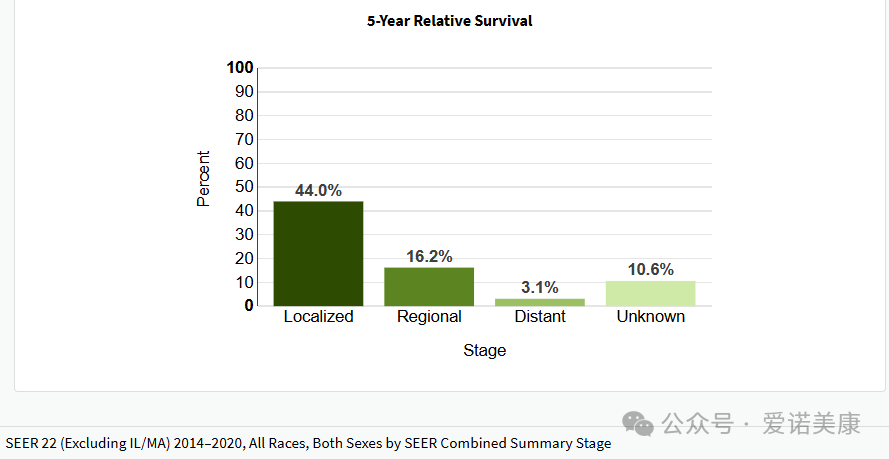
發布日期:2025-03-11轉移性胰腺癌治療選擇有限,常用的方案是FOLFIRINOX(亞葉酸、氟尿嘧啶、伊立替康和奧沙利鉑)、NALIRIFOX(伊立替康脂質體 [Onivyde]、奧沙利鉑、5-氟尿嘧啶 [5-FU] 和亞葉酸)以及吉西他濱+白蛋白結合型紫杉醇。已經擴散到附近結構或淋巴結(區域)的胰腺癌的五年相對生存率為 16.2%。
因為化療方案中國與美國逐漸統一,而且化療已經接近天花板,因此近年來有不少中國胰腺癌患者赴美就醫去尋求更前沿的藥物治療,愛諾美康梳理分析了近期胰腺癌患者參加的前沿臨床試驗。
RMC-6236在既往接受過治療的轉移性胰腺癌患者的III期研究
分期:III期臨床試驗
人數:460人
是否有對照組:有,是醫生選擇的標準化療方案
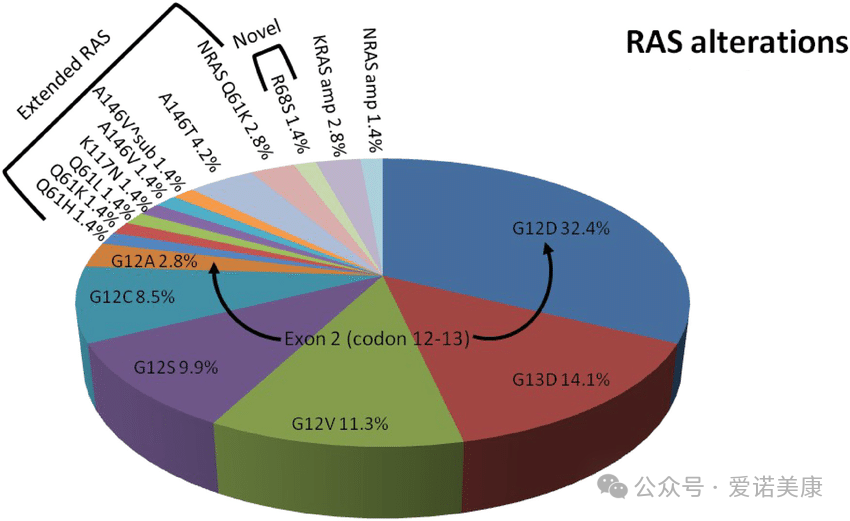
關鍵入組要求:符合條件的 RAS 突變,定義為 KRAS、NRAS 或 HRAS 中第 12、13 或 61 個密碼子(G12、G13 或 Q61)的非同義突變。
愛諾消息:目前愛諾已經有兩名胰腺癌患者在美入組,另一名患者正申請評估中;同時根據患者的申請經過以及美國主治醫生反饋的信息,目前試驗名額緊張。

RMC-6236 針對攜帶 KRAS 特定突變的晚期實體瘤患者的 1/1b 期多中心開放標簽研究
分期:I 期臨床試驗
人數:614人(所有實體瘤)
是否有對照組:無
關鍵入組要求:具有特異性 KRAS G12 突變(劑量遞增階段)或 RAS 突變【劑量優化/擴展階段;即KRAS、NRAS 或 HRAS 在密碼子 12、13 或 61(G12、G13 或 Q61)處的任何非同義突變】。
愛諾消息:試驗招募中。但胰腺癌已經提前開始進入III期臨床,因此I期臨床入組難度大。
RMC-9805 針對晚期 KRAS G12D 突變實體瘤患者的 1/1B 期、多中心、開放標簽研究
分期:I 期
臨床試驗人數:444人(所有實體瘤)
是否有對照組:無
關鍵入組要求:KRAS G12D 突變。
愛諾消息:一組為RMC-9805單藥治療組,一組為RMC-9805+RMC-6236劑量探索與擴展組。愛諾一名患者目前正進行入組評估。

IMM-1-104對既往接受過治療的 RAS 突變轉移性實體瘤患者一項 1/2a 期、開放標簽、多中心、非隨機、安全性和抗腫瘤活性研究
分期:I / II 期
臨床試驗人數:210人(所有實體瘤)
是否有對照組:無
關鍵入組要求:攜帶 RAS(KRAS、NRAS 或 HRAS)激活突變。
愛諾消息:IMM-1-104 單藥一線或二線治療胰腺癌;IMM-1-104 聯合改良吉西他濱和白蛋白結合型紫杉醇 (mGnP) 一線治療胰腺癌;IMM-1-104 聯合改良的 FOLFIRINOX (mFFX) 一線治療胰腺癌。
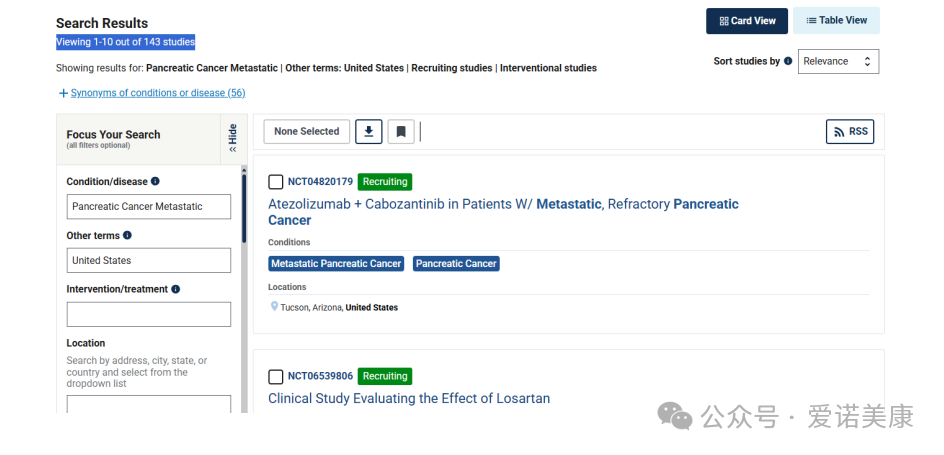
除上述臨床試驗外,美國臨床試驗官網顯示針對轉移性胰腺癌,美國正在招募的臨床試驗一共143項,有很多都是國內沒有的在研藥物。美國臨床試驗,沒有國籍限制,符合條件的患者均可入組,能夠為患者提供更多的治療選擇。





