丹娜法伯癌癥研究院:腦干腫瘤的CAR-T免疫治療
發布日期:2018-05-24丹娜法伯/波士頓兒童癌癥和血液疾病中心的、近有一項新的研究,研究團隊由Carl Novina博士和MarkKieran博士。他們的治療方法稱為“小分子CAR T細胞療法”。研究人員說,CAR T免疫療法前景很光明。而他們的這種CAR T免疫療法可以治療一系列的癌癥-包括侵襲性大、通常致命的童年腦癌——彌漫性內在腦橋腦膠質瘤,或DIPG(腦干腫瘤)。CAR T免疫療法專門靶向腫瘤細胞,同時降低威脅生命的副作用(例如,脫靶毒性和細胞因子釋放綜合征)。
他們的計劃是優化CAR T細胞療法的能力,使用患者的自己的基因修飾T細胞,以對抗癌癥,更精準地殺死腫瘤細胞,而不會引發稱為細胞因子釋放綜合征,不會引發免疫應答“風暴”。而研究的關鍵成分是一種獨特的小分子,它能極大地增強了治療中腫瘤靶向組分的特異性。
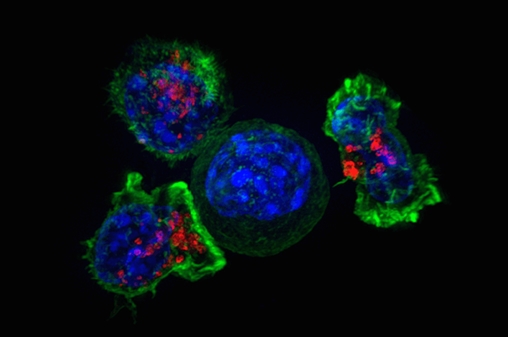
T細胞圍繞癌細胞。圖片來自美國國立衛生研究院。
“當大量免疫細胞被激活,并開始釋放炎癥信號,在整個免疫系統中進一步發出警報時,就會發生細胞因子的‘風暴’”Kieran博士說。“在傳統的CAR T細胞療法的情況中,T細胞殺死腫瘤細胞靶點的能力,通過遺傳得到增強,所以可能會進一步加劇免疫風暴。”自美國食品和藥物管理局FDA2017年8月作出了歷史性決定,批準CAR T細胞療法KYMRIAH用于急性淋巴細胞白血病(ALL)治療。急性淋巴細胞白血病是常見的兒童癌癥,而CAR T細胞療法KYMRIAH是進入美國市場的第一個基因療法。從那之后,一批同類的療法就一直備受關注。
治療DIPG的、更安全的CAR T細胞療法?
YMRIAH由諾華制藥制造,患者通過丹娜法伯/波士頓兒童基因療法計劃獲得這種治療。KYMRIA的工作機制是,通過修改患者的免疫細胞,來靶向并破壞ALL細胞上的CD19蛋白質。研究人員試圖在其他類型的癌細胞表面發現類似的蛋白質,但是這樣的蛋白質很難找到。“很少有腫瘤細胞有獨特的表面標記,就像ALL細胞上的CD19蛋白,”Novina博士說。“通常,正常細胞具有與腫瘤細胞相似的表面標記,所以很難在攻擊癌細胞的同時,不殺死健康細胞,而且不引發威脅生命的免疫應答。”
出國看病服務機構愛諾美康了解到,對于在兒童腦干中發現的DIPG這樣的癌癥,免疫風暴反應本身就可能是致命的。例如近,在加利福尼亞有一項針對DIPG的CAR T免疫治療,在小鼠中進行測試,能夠清除大部分DIPG細胞,但是在一些動物模型身上,導致“非常危險的腦腫脹”。盡管該療法將進入人體臨床試驗階段,但它對人類是否安全,研究人員尚不清楚。“每當談到腦腫瘤時,這種炎癥反應的影響可能很大。因為發生在腦部,在頭骨內,炎癥反應就變得更加危險,”Kieran說。
CAR T免疫療法的未來路線
所以Novina博士和Kieran博士想出了解決這個問題的方法,并開始使用小鼠模型,將愿景變為現實。他們計劃利用某些更常見于癌細胞的細胞表面標記物,來治療DIPG和其他癌癥。首先,他們將使用一種腫瘤靶向系統,該系統由小型人造分子構建,附著于抗體,能夠進入人體,并鎖定目標細胞表面標記物。
正常情況下,身體的非癌細胞會攝入這些分子,而腫瘤細胞比正常細胞更可能將這些“裝飾物”暴露在其細胞表面上。同時,專門準備的CAR T細胞將在實驗室準備就緒,目標是人造小分子。進入人體內之后,CAR T細胞就會發現小分子,并開始攻擊表面存在小分子的細胞。而腫瘤細胞的表面就有這類小分子,于是成為CAR T細胞攻擊的對象。
“重要的是,人體自身的免疫系統也將學會攻擊表面有這些小分子的細胞,使癌細胞腹背受敵”Novina博士說。Novina博士的首要任務是對小分子靶向系統做些微調。他打算與丹娜法伯 /波士頓兒童實驗室專門從事肉瘤小鼠模型的AllisonO'Neill博士合作。
然后,研究團隊將繼續使用DIPG小鼠模型,目標仍是大腦中的癌癥腫瘤靶點。“我們的研究不僅僅是為DIPG提供一種CAR T免疫療法,而是通過解決具挑戰性的兒童癌癥問題,然后制定靶向小分子CAR T免疫療法,治療無數其他種類的小兒和成人癌癥。”Novina博士說。






