專家破譯了白血病中一種非常規的功能機制
發布日期:2022-08-22盡管近年來罕見血癌的治療取得了重大進展,并且新藥已在德國獲得批準,但許多受影響個體的預后仍然不利。萊比錫大學醫學院的研究團隊正在開展幾個臨床前和轉化項目,以更好地了解這些疾病。研究人員正在研究骨髓癌是如何發展的。此外,他們發現了一種新的分子功能機制,并表明即使白血病細胞數量很少的患者也有很高的復發風險。
為什么高達 80% 的骨髓癌(多發性骨髓瘤)患者,在身體的某些部位會出現骨損傷(骨質溶解),而其他人卻沒有受到這種損傷?這是一個尚未充分研究的問題。在紐約布法羅的一次研究中,來自萊比錫的高級醫師 PD Maximilian Merz 博士,能夠證明惡性漿細胞引發骨損傷的細胞與體內其他細胞顯著不同。
使用計算機斷層掃描引導的穿刺,從溶骨中選擇性地收獲骨髓瘤細胞,并通過單細胞測序和其他技術進行研究。然后將獲得的樣本,與來自髂嵴的惡性漿細胞進行比較。骨髓穿刺通常在常規診斷中進行,以進一步調查惡性細胞。
Merz 博士和他的團隊能夠證明,來自溶骨的漿細胞會引發基因,這些基因除其他外,還能刺激骨降解破骨細胞并誘導新血管形成。“我們的研究結果強調了這樣一個事實,即骨髓瘤可以有許多面孔,并且多個不同的克隆可以同時出現在患者的多個位置,這將具有診斷性。”
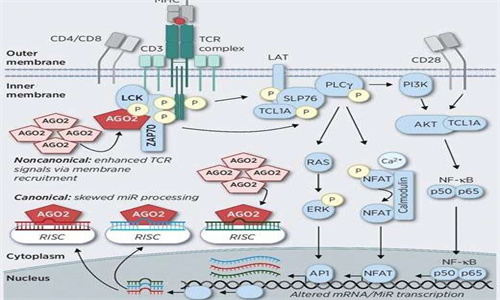
研究 T 淋巴細胞白血病的新功能機制,由 PD Marco Herling 博士領導的研究小組,發現了一種新的分子功能機制,這種機制是一種罕見且迄今為止研究很少的 T 淋巴細胞血癌形式。這種疾病很少對通常的血癌治療有反應,預后較差,患者平均存活率約為兩年。在他們的研究中,Herling 的團隊發現分子 AGO2 在這種罕見的血癌中起著至關重要的作用。
AGO2 以前被認為是一種關鍵的癌癥起始分子,它顯著參與了正常和腫瘤基因表達的精細調節。“在我們的研究中,我們能夠破譯 AGO2 在白血病細胞中的一種新的、非常規的功能機制,”Herling 博士說。然后補充說,“AGO2 直接與來自白血病細胞非常中心的生長因子的信號轉導的基本蛋白相互作用,AGO2 的存在增強了對傳入細胞信號的反應。使用各種蛋白質分析方法驗證了這種以前未知的分子相互作用,并確定了其高分子結構。這代表了一種治療干預的新醫學方法。”





