新型抗體偶聯藥,40-70%肺腺癌可能獲益
發布日期:2023-11-30根據 2 期 LUMINOSITY 試驗的頂線結果,Telisotuzumab vedotin (ABBV-399) 在EGFR受體野生型晚期/轉移性非鱗狀非小細胞肺癌 (NSCLC) c-Met 高和 c-Met 中表達的患者中,產生了令人鼓舞的總體緩解率 (ORR),分別為 35% 和 23%。
LUMINOSITY 是一項正在進行的、開放標簽的 2 期研究,旨在評估 telisotuzumab vedotin 在二線或三線環境中對具有高水平 c-Met表達的晚期/轉移性 EGFR 野生型非鱗狀 NSCLC 患者的療效和安全性。
該試驗招募了 270 名局部晚期或轉移性 NSCLC 患者,這些患者c-Met 陽性(免疫組化測定)、組織學記錄為非鱗狀EGFR野生型 NSCLC,并且在局部晚期或轉移性環境中接受過不超過 2 線的既往全身治療。研究人員正在評估 ORR 的主要終點以及 DOR、疾病控制率、無進展生存期和 OS 的次要終點。在 c-Met 高和 c-Met 中表達的EGFR野生型NSCLC 患者中,中位緩解持續時間 (DOR) 分別為 9 個月和 7.2 個月,中位總生存期 (OS) 分別為 14.6 個月和 14.2 個月。
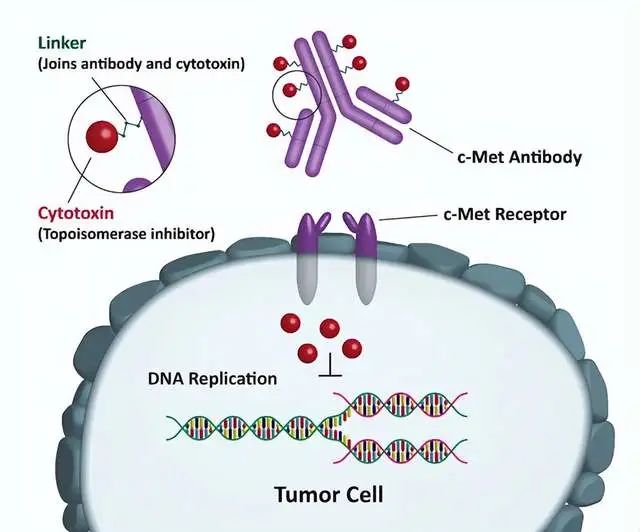
就安全性而言,telisotuzumab vedotin 沒有觀察到新的安全信號,并且該藥物的安全性與之前的發現一致。作為單一療法,telisotuzumab vedotin 通常耐受性良好。Telisotuzumab vedotin 是一種抗體藥物偶聯物 (ADC),靶向 c-Met,以微管蛋白抑制劑 MMAE 作為毒性有效載荷。c-Met 是一種在40-70% NSCLC 腫瘤中過度表達的受體酪氨酸激酶。
FDA 于 2023 年 1 月授予該藥物突破性療法稱號,用于治療 c-Met 高水平過度表達的晚期/轉移性EGFR野生型非鱗狀 NSCLC 患者,且這些患者在鉑類治療期間或之后疾病進展。除了 LUMINOSITY 之外,telisotuzumab vedotin 還在隨機 3 期研究 TeliMET NSCLC-01 中作為單一療法對既往接受過治療的 c-Met 過表達EGFR野生型非鱗狀 NSCLC 患者進行評估。





